Aos três anos de idade, Evan Lindberg foi diagnosticado com neuroblastoma, um câncer de infância que se desenvolve no tecido nervoso fora do cérebro. Naquela época, os tumores haviam se espalhado por seu pequeno corpo. Quimioterapia, radiação, imunoterapia e várias cirurgias se seguiram. “Por quatro anos, meu filho nunca teve um dia de folga”, diz o pai de Evan, Gavin. “Ele estava em tratamento ou recuperação. E freqüentemente a recuperação era pior que o tratamento”. Evan morreu em 2010 aos sete anos de idade.
Um dos médicos de Evan, o oncologista pediátrico Yael Mossé no Hospital Infantil da Filadélfia, na Pensilvânia, há muito tempo busca as opções de tratamento aprimoradas. Ela trabalha no neuroblastoma há mais de duas décadas, mas, apesar dos pequenos avanços, “realmente fizemos muito pouco progresso no desenvolvimento de terapias mais racionais ou direcionadas”, diz ela. Isso é verdade em geral para tumores sólidos na infância. Embora esses tumores sejam menos comuns do que câncer de sangue em criançaseles representam mais da metade das mortes associadas ao câncer em crianças de 0 a 14 anos1 nos Estados Unidos. Esses cânceres de infância diferem dos adultos em sua biologia e, portanto, requerem tratamentos distintos. No entanto, de mais de 180 medicamentos contra o câncer que receberam aprovação da Food and Drug Administration dos EUA (FDA) desde 2000, menos de uma dúzia foram desenvolvidos especificamente para crianças.

‘Proteínas escuras’ escondidas em nossas células podem manter pistas para o câncer e outras doenças
Mossé agora está colocando suas esperanças em moléculas fabricadas em laboratório que Sequestrar a maquinaria de disposição de proteínas da célula. Os medicamentos típicos roçam o fim dos negócios de uma proteína para inibir sua atividade. Protacs, abreviado para quimeras direcionadas à proteólise, eliminam completamente a proteína. Eles fazem isso ao amarrar proteínas associadas à doença em células humanas a uma enzima que marca a proteína para destruição.
Permitir esses encontros fatídicos – que a bioquímica Alessio Ciulli, na Universidade de Dundee, no Reino Unido, chama de proteína de “Kiss of Death” – expande a lista de possíveis alvos de drogas. Das aproximadamente 3.000 proteínas conhecidas por causar câncer e outras doenças, os medicamentos aprovados pelo FDA, por exemplo, têm como alvo menos de 700. A maioria do restante é considerada ‘industável’, porque não há bolso adequado no qual um medicamento possa anexar e bloquear a atividade da proteína. Mas um Protac apenas tem que agarrar; A maquinaria existente da célula faz o resto.
Pelo menos 30 Protacs entraram em ensaios clínicos desde 2019, quando os testes em humanos começaram, principalmente para câncer, mas também para a doença de Parkinson, distúrbios inflamatórios e dor. Os três mais avançados, para câncer de mamacâncer de próstata e leucemia, estão em ensaios de fase III, o último passo antes da aprovação do mercado. A maioria das proteínas degradadas que são direcionadas por medicamentos já aprovados.

Evan Lindberg, na foto à esquerda com seu pai Gavin, morreu de câncer aos sete anos de idade. Gavin agora é um advogado de pacientes, trabalhando com oncologista pediátrico Yael Mossé (à direita) e outros para desenvolver tratamentos para câncer de infância.Créditos: Wendy Lindberg, Hospital Infantil da Filadélfia
Mossé e seus colegas estão fazendo algo diferente – e mais arriscado – perseguindo proteínas do câncer que nunca foram drogadas antes. Ela lidera uma equipe que está desenvolvendo Protacs contra proteínas industráveis responsáveis pelo neuroblastoma e outros cânceres de infância, incluindo os do cérebro, fígado e osso. Todos os cânceres formam tumores sólidos. Mossé espera que os primeiros Protacs da equipe entrem em ensaios clínicos nos próximos dois anos.
Além disso, outros pesquisadores pretendem degradar proteínas que há muito são consideradas intocáveis, no câncer e além. “Mostrar que você pode segmentar algo novo com essa tecnologia será um momento crucial para o campo”, diz o químico Natanael Gray na Universidade de Stanford, na Califórnia, co-fundador da C4 Therapeutics, uma empresa farmacêutica de degradação de proteínas em Watertown, Massachusetts.
Mais do que um truque de laboratório
O primeiro Protac em funcionamento foi demonstrado em 2001, quando Craig Crews, um biólogo químico da Universidade de Yale em New Haven, Connecticut, o bioquímico Raymond Deshaies, no Instituto de Tecnologia da Califórnia em Pasadena, e seus colegas construíram um que degradou sua proteína -alvo no fluido celular a partir de ovos de sapos2. Na época, a maioria dos cientistas viu os Protacs como um truque de laboratório. Quando Ciulli começou a trabalhar com eles em 2009, os colegas “reviram os olhos”, ele lembra. “Eles disseram: ‘Protacs? Eles nunca serão drogas.’”
Um obstáculo precoce estava tornando os protacs pequenos o suficiente para penetrar nas células. Outro estava projetando -os para agarrar as mais abundantes e eficientes das enzimas conhecidas como ligases de ubiquitina. Essas enzimas, das quais existem cerca de 600 tipos, tag proteínas para destruição, conectando cadeias de proteínas muito menores chamadas ubiquitinas (ver ‘proteína eliminada’). Após um grande esforço, três trabalhos em 2015 revelaram protacs potentes que quase eliminaram completamente as proteínas -alvo em células e camundongos3–5. “Depois desses documentos, não havia dúvida de que poderíamos degradar proteínas”, diz Ciulli. “Agora todo o mundo dos alvos poderia se abrir.” Um co-autor de um dos jornais, Ciulli mais tarde ajudou a fundar a Anphista Therapeutics, uma empresa de degradação de proteínas em Cambridge, Reino Unido.
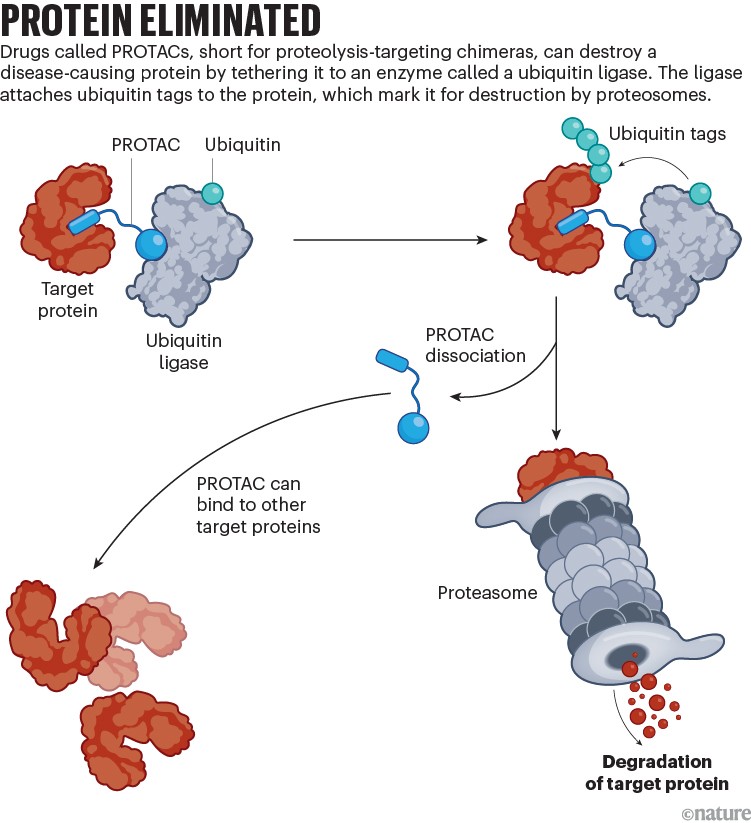
Os artigos destacaram uma vantagem fundamental dos Protacs. Enquanto os medicamentos convencionais devem residir em uma proteína causadora de doenças, os Protacs se envolvem com seu alvo brevemente, enviam-o para destruição e avançam para o próximo alvo. Esse recurso de captura e liberação significa que doses muito pequenas podem durar muito tempo. Outra vantagem é que os Protacs não levam prisioneiros. Algumas proteínas contribuem para uma doença de várias maneiras, mas, ao eliminar completamente a proteína, um Protac elimina todas as contribuições possíveis.
Os artigos de 2015 estabeleceram Protacs como uma próxima onda de drogas. “Eu nunca vi uma tecnologia que foi mais amplamente adotada, tão rapidamente”, diz Gray. “Não são apenas poucas biotecnologia arriscada. Todas as empresas farmacêuticas têm programas de degradantes avançados”.
Este cientista tratou seu próprio câncer com vírus que ela cresceu no laboratório
Tudo isso aconteceu tarde demais para Evan Lindberg. Em 2010, seu pai entrou nele em um dos ensaios clínicos de Mossé, testando um medicamento existente contra uma proteína frequentemente corrompida no neuroblastoma. O câncer de Evan não respondeu. O tumor também continha cópias extras do gene para uma proteína que é um fator notório de câncer de infância, o fator de transcrição Mycn. O MYCN liga os genes para fazer as células replicarem durante o desenvolvimento da infância. Muito disso pode transformar cânceres curáveis em assassinos agressivos através de um crescimento não controlado. Mas fatores de transcrição como o MYCN são considerados indrubáveis.
Em uma reunião sobre o MYCN em 2019, Mossé percebeu que os Protacs poderiam ser uma solução. Um dos fundadores da empresa Protac Nurix Therapeutics em São Francisco, Califórnia, participou da reunião e “realmente nos motivou a pensar na degradação direcionada de proteínas e a ir atrás do MYCN, para tentar realmente fazer algo grande”, diz Mossé. Armada com uma concessão de fundação privada, ela começou a trabalhar com Nurix. O trabalho expandiu-se em 2024, quando uma equipe Mossé se reuniu junto com o bioquímico Martin Eilers na Universidade de Würzburg, na Alemanha, ganhou uma grande concessão da Cancer Grand Challenges, uma iniciativa global sem fins lucrativos que procura enfrentar tumores sólidos na infância.
A equipe, chamada Koodac, por derrubar motoristas oncogênicos e curar câncer de infância, também inclui cientistas do Reino Unido, Áustria e França e defensores dos pacientes em cinco continentes. Entre eles estão Gavin Lindberg e sua esposa Wendy, que, depois que Evan morreu, estabeleceu uma fundação de caridade que, na última década, financiou uma posição de pesquisa no laboratório de Mossé. A equipe está perseguindo o MYCN e outros quatro alvos de proteínas. O objetivo é encontrar medicamentos que não apenas funcionam, mas também são mais convenientes do que infusões de hospitais e baratos o suficiente para compra em países de baixa e média renda, onde as famílias geralmente precisam renunciar ou abandonar o tratamento por causa do custo.
Matando os assassinos da infância
Três das proteínas que a equipe de Koodac está direcionando resultado de um tipo de erro genético que geralmente está presente no câncer. A travessia, a quebra e a reparação dos cromossomos podem dar origem a um novo gene híbrido – uma fusão de genes – que possui sequências de ambos os genes originais. As proteínas de fusão resultantes são a causa direta de muitas leucemias, linfomas e tumores sólidos na infância. Duas dessas proteínas de fusão impulsionam o sarcoma de Ewing e a rabdomiossarcoma, devastando os ossos da infância e os cânceres de tecidos moles. O terceiro causa um raro câncer de fígado.
À medida que as células tumorais evoluem, as proteínas de fusão persistem, tornando -as alvos atraentes, diz Charles Mullighan, um hematologista do Hospital de Pesquisa Infantil St. Jude em Memphis, Tennessee. Mullighan e seus colegas fabricam e testam protacs e degradantes de proteínas semelhantes para câncer de sangue na infância e tumores cerebrais. Quanto a se os degradantes de proteínas podem curar esses cânceres, “existe o potencial”, diz Mullighan. Mas ele acrescenta que um medicamento pode não ser suficiente. “Os cânceres são astutos e podem encontrar maneiras de contornar isso.”
Além de Koodac, duas outras equipes de grandes desafios do câncer estão enfrentando tumores sólidos na infância. Uma equipe reúne pesquisadores de nove instituições da Europa e dos Estados Unidos para trabalhar em degradantes de proteínas e terapias celulares. O outro, que inclui investigadores de oito instituições nos Estados Unidos, Reino Unido e França, está focado exclusivamente em terapias celulares. Tais colaborações acadêmicas amplas são essenciais para progredir no câncer de infância, dizem os pesquisadores. “Para cânceres apenas pediátricos, o mercado é tão pequeno que não se encaixa no plano de comercialização de uma empresa farmacêutica tradicional”, diz Catherine Bollard, co-líder da equipe de terapia celular e hematologista pediátrica do Hospital Nacional Infantil em Washington DC.
O universo protetível
Nenhum protacs ainda foi aprovado. O primeiro a entrar nos ensaios da Fase III, vepdegestrant, desenvolvido por Arvinas em New Haven, Connecticut, degrada o receptor de estrogênio no qual a maioria dos cânceres de mama se baseia em crescimento. No início de março, Arvinas e seu parceiro, Pfizer, relataram que o degradador era melhor do que um medicamento anti-oestrogênio padrão ao permitir que os participantes do julgamento cujos tumores tivessem uma mutação comumente associada ao câncer de mama para viver mais sem o agravamento da doença (embora não tenha se saído melhor em uma análise que incluiu todos os participantes do ensaio). “Planejamos compartilhar dados (de estudo) com as autoridades regulatórias globais para apoiar potencialmente os registros regulatórios”, escreveu o diretor médico de Arvinas, Noah Berkowitz, em um e-mail para Natureza. Dois outros ensaios de fase III vepdegestrant estão em andamento.
Enquanto isso, dois outros Protacs atingiram ensaios de Fase III. Um degrada o receptor de androgênio que impulsiona a maioria dos cânceres de próstata metastáticos; O outro, a enzima BTK exigida por leucemias linfocíticas crônicas. Os medicamentos contra esses alvos já estão disponíveis, mas os cânceres avançados inevitavelmente se tornam resistentes a eles.
